|
Coënzymen:
Coënzymen zijn
organische verbindingen ( reagentia) die een enzym nodig heeft om een
bepaalde reactie te kunnen uitvoeren.
Coënzym: een
voor de activiteit van een enzym onmisbare factor, die met het
eiwitgedeelte van een enzym geassocieerd is.
De coënzymen zijn
verbindingen met een relatief laag molecuulgewicht, die gemakkelijk
diffunderen door een membraan dat eiwitmoleculen tegenhoudt. Bovendien
zijn de coënzymen bestand tegen verhitting in waterige oplossing, terwijl
de eiwitcomponenten dan irreversibel denatureren.
Het coënzym is bepalend
voor het type reactie dat een enzym zal katalyseren, maar de
eiwitcomponent bepaalt welke verbinding deze reactie kan ondergaan
( specificiteit ).
Vitamines ( met name
de in water oplosbare ) zijn veelal voorstadia van coënzymen, sommige
vitamines zijn zelf coënzym.
Coënzym A:
Brutoformule: C21H36N7O16P3S
Coënzym A werd in 1945 door Fritz
Albert Lipmann ontdekt , die voor deze ontdekking in 1953 een Nobelprijs
kreeg. (
autobiografie )
Coënzym A is opgebouwd uit een cysteamine-eenheid,
een pantotheenzuurfragment en adenosinedifosfaat.
Het chemisch
actieve gedeelte van dit coënzym is de thiolgroep, vandaar dat het vaak
wordt afgekort als CoA-SH.
Het lange CoA-gedeelte van CoA-SH dient om goede bindingsinteracties aan te gaan met
de enzymen die van dit coënzym gebruik maken.
Het thiolaatanion
is door zijn goede polariseerbaarheid een zeer goed nucleofiel en
bovendien een zeer goede vertrekkende groep. Deze eigenschap
maakt coënzym A bijzonder geschikt om op te treden in omesteringsreacties.
Bekend is de
werking van acetylcoënzym A in de biosynthese van vetzuren. Acetylcoënzym
A treedt op als algemeen reagens voor acetyloverdracht op talrijke
plaatsen in de cel. Coënzym A speelt een centrale rol in het
metabolisme van vetten, koolhydraten en eiwitten waarvan de afbraak
plaatsvindt via acetyl-CoA ( citroenzuurcyclus). CoA is ook betrokken bij
de biosynthese van vetzuren en bij acetyleringsreacties, zoals de vorming
van acetylcholine.
De acetylering van
CoA-SH tot acetyl-S-CoA door de energieke verbinding acetylfosfaat wordt
gekatalyseerd door het enzym fosfotransacetylase.
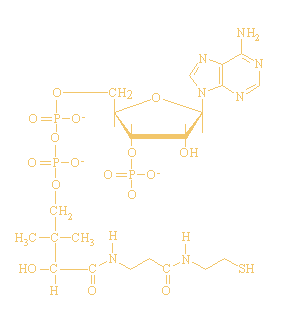
Coënzym A
Nicotinamide Adenine Dinucleotide ( NAD+
)
Bruto formule: C21H28N7O14P2
Dit
is een verbinding die bestaat uit nicotinezuuramide-, ribose-, pyrofosfaat-
en adeninemoleculen.
NAD+ is de
belangrijkste elektronenacceptor bij de oxidatie van brandstofmoleculen.
De gereduceerde
vorm van NAD+ is NADH.
Dit NADH wordt via de elektronentransportketen weer
geoxideerd, waarbij het energierijke ATP ( adenosine tri-fosfaat)
opgebouwd wordt.
Wanneer het coënzym is betrokken bij de opbouw
van stoffen tijdens de biosynthese, bevat het een extra fosfaatgroep op de
2’-plaats van ribose (NAD+ en NADPH).
Bij de biosynthese van de vetzuren bijvoorbeeld,
worden de vier elektronen die nodig zijn voor de reductie van een carbonylgroep tot een methyleengroep, geleverd door twee moleculen NADPH.
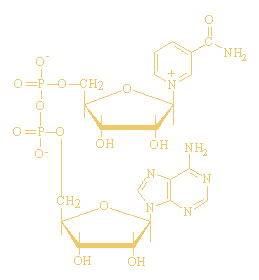
Nicotinamide Adenine Dinucleotide ( NAD+
)
Flavine Adenine Dinucleotide ( FAD ); Flavine Adenine
Mononucleotide ( FMN)
Bruto formule FAD: C27H33N9O15P2
Bruto formule FMN: C17H21N4O9P
FAD en FMN zijn
belangrijke coënzymen in enzymatische redoxreacties.
De coënzymen zijn
enzymatisch gemodificeerde versies van vitamine B2 ( Riboflavine) en
bevatten als chemisch actief deel het flavinefragment ( de
isoalloxazinering).
De flavine-ring
dankt zijn naam aan het Latijnse woord flavius dat geel betekent.
Verbindingen met het flavinefragment zijn als vaste stof en in neutrale
oplossing helder geel.
Het vitamine
riboflavine wordt enzymatisch in twee actieve coënzymvormen omgezet.
Fosforylering op de
5’-OH van de ribitylgroep geeft FMN.
Adenosinylering van
FMN geeft FAD.
FAD treedt onder
andere op als elektronenacceptor in oxidaties van alkanen naar alkenen
waarbij FAD gereduceerd wordt tot FADH2.
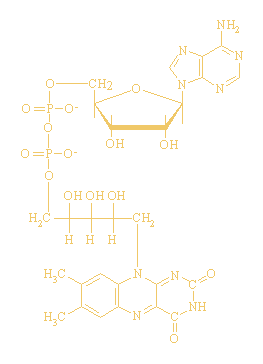 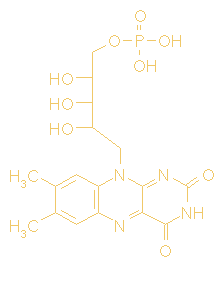
Flavine Adenine Dinucleotide en Flavine Adenine
Mononucleotide
Thiaminepyrofosfaat
Bruto formule: C12H19ClN4O7P2S
Thiaminepyrofosfaat
is opgebouwd uit thiamine ( vitamine B1) en een
pyrofosfaatgroep.
De pyrofosfaatgroep fungeert als geladen groep voor
bindingsinteracties met de enzymen die van dit coënzym gebruik maken.
Het thiaminedeel bestaat uit een pyrimidine- en een thiazoliumring, verbonden
via een methyleengroep.
Het coënzym is
behulpzaam bij de enzymatische decarboxilering van α-ketozuren .
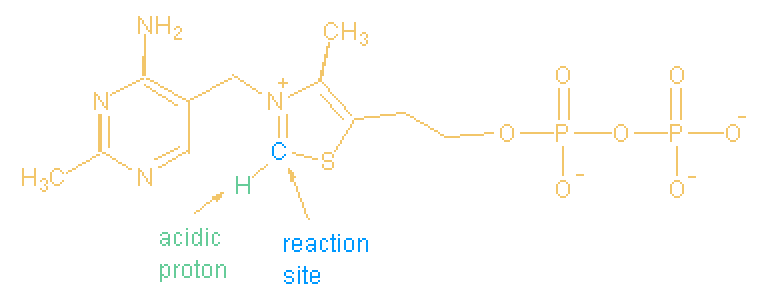
Thiaminepyrofosfaat
Pyridoxaalfosfaat
Bruto formule: C8H10NO6P
Het coënzym
pyridoxaalfosfaat wordt opgebouwd uit vitamine B6 (pyridoxine).
Pyridoxaalfosfaat is een coënzym voor een groot aantal verschillende
enzymen die betrokken zijn bij de chemische veranderingen op de α,ß en
γ
plaats van de natuurlijke α-aminozuren.
Enzymen die met behulp van pyridoxaalfosfaat werken, vallen in een van de volgende vier klassen;
aminotransferasen
decarboxylasen
racemasen
lyasen.
De reactie tussen
aminozuren en de pyridoxaalfosfaat bevattende enzymen verloopt via de
positief geladen iminiumverbindingen.
Voorbeelden hiervan
zijn de transaminering van aminozuren en de decarboxylatie van aminozuren.
In alle gevallen is
de functie van het pyridoxaalfosfaat die van een energetisch gunstige
elektronenput waardoor de carbanionen gestabiliseerd worden die tijdens de
enzymatische reacties gevormd worden.

Pyridoxaalfosfaat
Coënzym B12
Synoniemen voor dit coënzym
zijn: Cobamide coenzyme; Adenosylcobalamin; Deoxyadenosylcobalamin;Cobamamide; Vitamin B12 coenzyme; Calomide;
Cobalamin coenzyme
Brutoformule C72H105CoN18O17P
Coënzym B12,
een vorm van vitamine B12, is een kobaltbevattend coënzym met
een complexe structuur. Het bevat een gemodificeerd porfirineringssysteem.
Naast bindingen met de pyrroolgroepen in het porfirineringssysteem kan
kobalt nog twee andere liganden binden, loodrecht op het vlak van het
ringsysteem.
Afhankelijk van de cellulaire functie van coënzym B12
kunnen verschillende groepen verbonden worden.
In enzymatische
reacties is coënzym B12 vooral actief als katalysator bij
omleggingen van 2-methylmalonzure ester naar barnsteenzure ester.
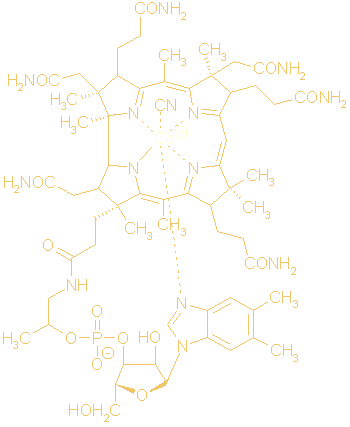
Coënzym B12
Tetrahydrofolaat
Bruto formule: C19H23N7O6
Het coënzym
tetrahydrofolaat is afkomstig van het vitamine foliumzuur.
Het is als
coënzym betrokken bij de vorming van C-C bindingen waarbij een fragment
van één koolstof atoom wordt overgedragen.
Het één-koolstoffragment dat
door tetrahydrofoliumzuur ( FH4) wordt overgedragen is gebonden
aan N-5, N-10 of aan beide.
De koolstofeenheid kan voorkomen in drie
oxidatietoestanden: de meest gereduceerde vorm ( de methylgroep, -CH3),
een tussenvorm ( de methyleengroep,-CH2-) en de meest
geoxideerde vorm ( de formylgroep,-CHO).
De hoogst geoxideerde vorm van
koolstof, CO2, wordt door biotine overgedragen en niet door FH4.
Door enzymatische redoxreacties zijn de verschillende oxidatievormen van
het één-koolstoffragment in elkaar om te zetten.
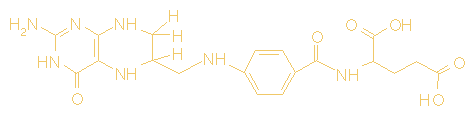
Tetrahydrofolaat
Biotine
Bruto formule: C10H16N2O3S
Biotine ( een
enkele maal aangeduid als vitamine H) wordt in de biosynthese toegepast
als coënzym op plaatsen waar CO2 wordt overgedragen.
Een
voorbeeld van waar dit gebeurt, vinden we in de biosynthese van vetzuren
waar acetyl-CoA wordt omgezet in malonyl-CoA. Dit proces wordt
gekatalyseerd door het enzym acetyl-CoA-carboxilase dat gebruik maakt van
biotine als coënzym. Het biotine is hierbij covalent gebonden aan de ε-aminogroep
van een lysineresidu van het enzym.
Bij de carboxylering van acetyl-CoA
wordt eerst een carboxy-biotine intermediair gevormd. De geactiveerde CO2-groep
wordt daarna overgedragen naar acetyl-CoA, waarbij malonyl-CoA wordt
gevormd.
Biotine wordt in voldoende mate aangemaakt door bacteriën in de
dikke darm.
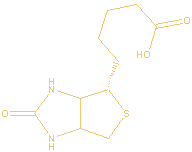
Biotine
ATP
Bruto formule: C10H16N5O13P3
Synoniem:ATP; adenosine 5'-triphosphate; dATP;
5'-adenylate triphosphate; 5'-rATP; rATP; 5'-dATP; 5'-deoxyadenylate
triphosphate; deoxyadenosine 5'-triphosphate; deoxyadenosine triphosphate;
Adenosine 5'-triphosphate disodium salt (ATP).
Adenosinetrifosfaat ( ATP ) is een
nucleotide ( stof opgebouwd uit een stikstofrijk molecuul (( purine - of
pyrimidine-base )) , een suikermolecuul en fosforzuur ) dat als co-factor
bij vele enzymatische reacties in het lichaam wordt gebruikt.
ATP wordt
uit adenosinedifosfaat ( ADP ) gevormd bij de oxidatie van suikers,
eiwitten en vetten en wordt verbruikt bij energiebehoevende processen in
de cel.
ATP wordt vaak het " universele
betaalmiddel" genoemd voor de cellulaire energie. Het is voor de cellen
een geriefelijke manier om energie op slaan die de cellen nodig hebben om
proteïnen te synthetiseren, of voor het kopiëren van DNA, en de opbouw van
nieuwe organellen.
ATP is ook nodig voor bijvoorbeeld de spiercontractie,
het pompen van water door membranen en de verplaatsing van cellen.
Naast de energievoorziening helpen
mitochondriën ook bij de regulatie van concentraties calcium en andere
elektrisch geladen deeltjes in het cytoplasma. Ook recyclen zij- en breken
zij de energie in vetzuren en aminozuren af .
Hoewel de mitochondriën al vanaf het
jaar 1880 onderzocht worden, duurde het vele jaren voordat wetenschappers
het functioneren van dit organel begrepen.
Het proces waarbij de
mitochondriën zuurstof gebruiken om de chemische energie , die is
opgeslagen in voedsel, vrij te maken , wordt cellulaire ademhaling
genoemd. ( cellular respiration ).
In de vroege jaren 1900 werd ontdekt
dat de biochemische reacties van dit type ademhaling in twee hoofdgroepen
vallen : het koolstof traject , waarin suiker wordt afgebroken tot
kooldioxide en waterstof ; en het waterstof traject waarbij waterstof in
stappen wordt omgezet in zuurstof , waarbij water wordt gevormd en energie vrijkomt.
In het waterstof traject passeren de
elektronen van waterstof de " elektronen transportketen " . Deze
elektronen transportketen bestaat uit 5 enzymcomplexen. Tijdens het
transport van deze elektronen door de elektronen transportketen, geven de
elektronen een deel van hun energie af. Deze energie wordt dan opgeslagen
in moleculen ATP. Aan het einde van de keten zijn voor elke molecuul
suiker, 38 moleculen ATP gevormd.
Soms wordt een totaal van 36 ATP aangehouden,
omdat bekend is dat in eukaryote cellen het gereduceerde NAD, dat gevormd
is door de glycolyse in het cytoplasma, actief getransporteerd moet worden
over de mitochondriële membraan om beschikbaar te komen voor de
elektronentransportketen. Het actieve transport over het membraan kost 1
ATP voor elk NADH dat getransporteerd wordt. Wanneer men zo wil redeneren
, moet men ook het actieve transport van andere moleculen in ogenschouw
nemen. ( pyruvaat ? , fosfaat ? , Mg+ etc ). Het juiste netto
resultaat van ATP is onbekend , maar moet worden beschouwd als minder dan
36.
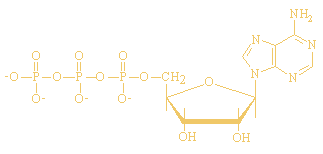
ATP
GTP
Bruto formule:
C10H16N5O14P3
Guanosine trifosfaat: synoniemen: Guanosine 5'-triphosphate,
disodium salt; GTP dihydrate; 5'-guanylate triphosphate; 5'-rGTP; GTP;
guanosine triphosphate; rGTP; guanosine-5-triphosphate disodium salt.
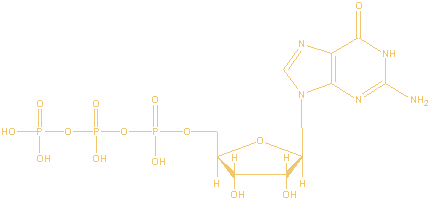
GTP
|

